
生活垃圾焚烧发电时,烟气中产生的产要污染物有酸性气体、烟尘、重金属等物质,不同的污染物需要装备不同的处理技术、工艺和设备。例如,针对烟气中产生的酸性气体,其主要成分由SOx(硫氧化物)、NOx(氮氧化物)、HCl(盐酸)等组成,其中NOx的去除原理为化学还原反应(SNCR或SCR技术);而SOx、HCl的去除原理为酸碱中和反应。本文重点介绍SOx、HCl的去除方法及工艺技术经济比较。
一.酸性气体SOx、HCl的来源及含量
生活垃圾焚烧烟气中的SOx主要由SO2构成,产生于原生垃圾中含硫化合物焚烧氧化所致(主要为有机硫,也有部分源于无机硫)。HCl来源于原生垃圾中的氯化物含量,如塑料、橡胶、皮革、纸张(氯漂白所致)、餐厨垃圾含氯农药残留、,厨余中的NaCl以及KCl等。与燃煤火力发电厂不同的是:垃圾焚烧烟气中SOx的含量很低,一般为200-800mg/Nm3,质量百分含量约为0.11%;而HCl的含量又较高,达200-1600mg/Nm3(在我国,由于塑料制品的大量应用,致使烟气经处理后截留在飞灰中的氯元素含量甚至高达25%),一般生活垃圾产生的SOx是HCl的1/10以下,所以HCl是垃圾焚烧烟气中主要的污染气体。
二.反应原理
1.氯化氢(HCl)
聚氯乙稀PVC的热稳定性较差,140℃时就开始分解出HCl,反应温度达600-800℃,反应时间10-15min时;化学反应原理为:
CH2CHCl+5/2O2=2CO2+HCl+H2O
氯化钠反应温度为430-540℃,反应原理为:
2NaCl+SO2+1/2O2+H2O=Na2SO4+2HCl
2NaCl+2SiO2+H2O=Na2O(SiO2)2+2HCl
2NaCl+4SiO2+Al2O3+H2O=NaO2(SiO2)4 Al2O3+2HCl
2.硫氧化物(SOx)
燃烧过程中,当过量空气系数小于1时,有机硫的反应产物有SO2及H2S、SO等;当过量空气系数大于1时即完全燃烧条件下,95%以上生成物为SO2,约有0.5-2%的SO2进一步反应生成SO3。另外,研究表明:在1127℃的高温燃烧条件下,几乎不生成SO3,但过量空气系数大于1的燃烧条件下,SO3的生成为迅速增加。
有机硫的反应机理:
CxHyOzSp+O2=CO2+H2O+SO2+未完全燃烧物
2SO2+O2=2SO3
无机硫的反应机理:S+O2=SO2
三.HCl的危害
HCl气体对眼和呼吸道黏膜有较强的刺激作用,引起胸部窒息感,咳嗽、咯血、肺水肿、直至死亡;
HCl气体会对余热锅炉受热面和监测仪表产生高低温腐蚀,影响余热锅炉安全并限制了过热蒸汽参数的提高;
HCl气体的存在升高了烟气露点,导致排烟温度升高,降低锅炉热效率 ;
氯源在一定条件下与重金属反应生成低沸点的金属氯化物,从而加剧了重金属的挥发,导致重金属在飞灰上的富集,增加飞灰毒性 ;
HCl气体能促进氯酚、氯苯、氯苯并呋喃等“三致”有机物的生成,而且PVC裂解后生成的HCl被认为能促进多环芳烃(paHs)的生成。因此,有效去除HCl气体直接关系到焚烧系统的安全和环保运行。
四.SOx、HCl的去除方法
酸性气体SOx、HCl主要通过干法、半干法、湿法等净化工艺加以去除:
1.干法脱酸:
干法脱酸的基本原理为:
CaO+SO2=CaSO3
CaO+2HCl=CaCl2+H2
干式脱酸有2种方式。一种是干性药剂(一般采用消石灰)和酸性气体在反应塔内进行反应;另一种是在进入除尘器前的烟气管道中喷入干性药剂,在此与酸性气体反应。消石灰与酸性气体发生中和反应要有合适温度(140~170℃),而余热锅炉出口的烟气温度往往高于这个温度,为提高脱酸效率,一般需通过喷水降低烟温。
减温塔:从锅炉出来的温度为190~200℃的烟气进入减温塔。减温塔由冷却装置与飞灰排出装置组成。冷却水由冷却水供应泵从水箱送至喷嘴,并被压缩空气雾化后喷入减温塔内与烟气直接接触。减温塔的高度设置应确保喷入的雾化水可以完全蒸发,直径设置应能防止塔内壁被雾化的水微粒接触。烟气经减温塔降温至150℃左右后进入后续设备。烟气中部分粉尘落入塔底的料斗中,经排灰阀、输送机送至飞灰贮仓。减温塔底部需配置加热装置,防止飞灰吸潮沉积在内壁上腐蚀减温塔。
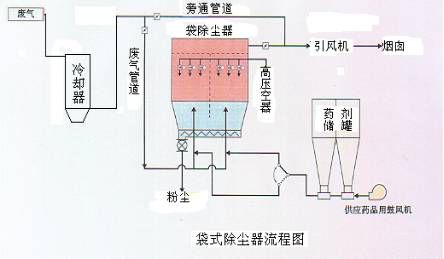
2.半干法脱酸:
半干法脱酸的基本原理为:
2HCl+Ca(OH)2=CaCl2+2H2O
SO2+Ca(OH)2=CaSO3+H2O
半干法脱酸装置一般设置在除尘器之前,主要包括给料系统、混合系统和反应系统。脱酸剂CaO在给料系统制作成粉状,再进入制浆系统与水充分混合制成石灰浆,最后以喷雾状进入反应系统。HCl、SOx等酸性成分被中和,生成中性的细小固体颗粒,随烟气进入下一步净化系统。
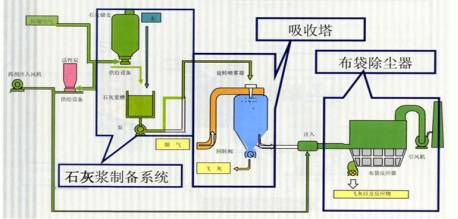
3.湿法脱酸:
湿法脱酸装置设置在除尘器之后,从袋式除尘器出来的温度约140℃的烟气经底部进入湿式洗涤塔。洗涤塔分为冷却部和吸收减湿部。烧碱稀释槽中配制好的烧碱溶液通过烧碱输送泵、冷却液循环泵送至冷却部上方的喷嘴,向下喷入与逆流的烟气充分接触,将烟气温度降至饱和温度。同时,在此过程中烧碱溶液与烟气中的部分酸性气体进行反应。塔底的吸收液一部分循环使用,一部分排出以降低溶液中的含盐量以保证酸性气体的吸收率。
烟气经冷却和吸收后进入洗涤塔上部的吸收减湿部。减湿水与烧碱溶液一并由减湿水循环泵输送至减湿部上方喷嘴,向下喷入并均匀地经过填料床与烟气充分接触,酸性气体被进一步去除。反应后的减湿水从吸收减湿部下部排入减湿水槽。净化后的烟气经塔顶除雾器除雾后进入烟气再加热系统。
烟气再加热器:从湿式洗涤塔出来的烟气温度约有70℃,为防止低温腐蚀及烟囱出口冒白烟,需将烟气加热至150~160℃才能排放。再加热方式可选择蒸汽加热或电加热(一般选用蒸汽加热)。从烟气再加热器出来的烟气通过引风机经烟囱排入大气。
采用消石灰Ca(OH)2作为溶剂时,浓度为10-30%,具有价格低、溶解度低的特征,但生成的石膏容易导致填料及管道堵塞与结垢,因此,湿法工艺更多采用NaOH溶剂,浓度为10-20%。与消石灰相比,苛性钠价格高,但与酸性气体的反应速率高,吸收效果好且用量小,因此目前较多采用苛性钠溶剂,主要反应过程为:
HCl+NaOH=NaCl+H2O
SO2+2NaOH=Na2SO3+H2O
Na2SO3+O2=Na2SO4
SO3+2NaOH=Na2SO4+H2O
欧洲采用湿法烟气净化的焚烧厂实验数据调查表明:PH值为5-6的SO2吸收阶段,NaOH所吸收SO2的量远高于预期值。

需要说明的是:湿法去除率虽然较高,但流程复杂,配套设备较多,投资较高;产生高浓度无机氯盐及重金属的废水,需经处理后才能排放;处理后的废气因温度降低至露点以下,需再加热以防止烟囱腐蚀及形成白烟现象。
五.脱酸净化工艺特性综合比较
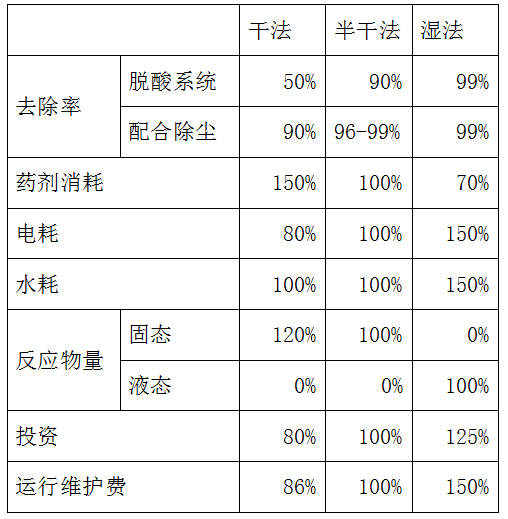
注:1.去除率以HCl去除率为基准;2.药剂种类:干式为Ca(OH)2粉(95%纯度);半干式为Ca(OH)2乳液(15%纯度)。
六.几种工艺烟气脱酸综合比较结果
1.脱酸效率:湿法>半干法>干法;
2.水消耗:湿法>半干法>干法;
3.原料消耗(按消石灰计):干法>半干法>湿法;
4.电耗:湿法>半干法>干法;
5.投资:湿法>半干法>干法;
6.维护费:湿法>半干法>干法。
七.倡议
生活垃圾焚烧时烟气中的主要酸性污染物为盐酸,盐酸来源于原生垃圾中含氯物质或材料,其中每个家庭、单位、团体等日常用于装载垃圾的一次性塑料袋占据了含氯材料的大部分比例(其它具备回收价值的含氯包装品、纸张等被“垃圾分类”或是拾荒者提前捡走)。那么,有没有能够代替一次性塑料垃圾袋的、价格低廉的、无氯或低氯的物品用于装载家庭日常生活垃圾?为此提出一种技术研发的思路和方向:利用田间每年产生的、无法充分消纳掉的农作物秸秆,例如玉米秸秆、小麦秸秆、稻米秸秆等,通过简单的加工、制膜过程,制作成适于使用的一次性垃圾袋,用于代替传统的一次性塑料袋?如果这一技术得到突破,不仅能够大面积避免田间露天焚烧秸秆、污染环境的现象,而且能够提高垃圾热值、大幅降低焚烧后烟气中的氯产生量、从而降低烟气脱酸处理成本。。。。。。我们拭目以待,并希望有识之士能在这个领域进行有益的探索。
 垃圾焚烧发电烟气中酸性污染物的去除…
垃圾焚烧发电烟气中酸性污染物的去除… 小城镇垃圾处理模式研究综述
小城镇垃圾处理模式研究综述 生物质能开发利用应用节能技术
生物质能开发利用应用节能技术 一篇文章带你读懂海螺水泥协同处置
一篇文章带你读懂海螺水泥协同处置 垃圾焚烧发电厂汽轮机特点及热力系统…
垃圾焚烧发电厂汽轮机特点及热力系统… 机械加工类项目污染防治措施
机械加工类项目污染防治措施 生活垃圾焚烧发电为什么能够减少温室…
生活垃圾焚烧发电为什么能够减少温室… 没有运动部件的风水联合冷渣器常见故…
没有运动部件的风水联合冷渣器常见故… 生活垃圾的危害及其处理
生活垃圾的危害及其处理 污泥处理的3种方式介绍
污泥处理的3种方式介绍 畜禽粪便无害化处理
畜禽粪便无害化处理 垃圾焚烧炉渣综合利用项目的技术及管…
垃圾焚烧炉渣综合利用项目的技术及管… 生活垃圾分类的立法与落实建议
生活垃圾分类的立法与落实建议 危废处理四道难题怎么解决?
危废处理四道难题怎么解决? 关于工业固体废物综合利用的探讨
关于工业固体废物综合利用的探讨 我国餐厨垃圾处理分析及方法对比
我国餐厨垃圾处理分析及方法对比